Hogy az átalakítás a kémiai energia elektromos
Átalakítása kémiai energiát elektromos energiává társított a jelenség a elektrolitos disszociáció, amelynek lényege abban áll, a kialakulását a töltött részecskék - ionok, amikor feloldjuk neko-toryh anyagok (savak, sók, stb).
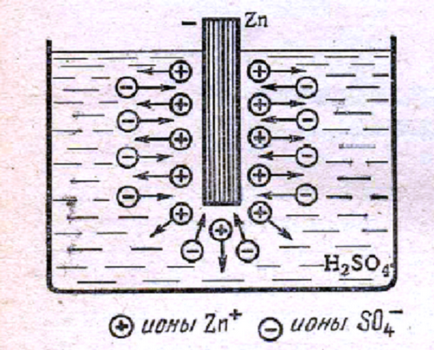
Ábra. 1 cinklemezt kénsavas oldat.
Ábra. Az 1. ábrán egy cink lemez, süllyesztjük vizes kénsav oldat (elektrolit). Cink feloldódik az elektro-Lite, az oldatot átvisszük a szex-ionok voltak Zn +. Az oldatot hátba Xia pozitív és cink - negatív, de. cink oldódási miatt
kémiai erők.
Az érintkező felület cink - oldatot egy elektromos mező előállított ionok irányított ápollószerek tolvaj cink.
Mivel a kioldódási cink növeli a töltés, és a velük együtt az elektromos mező. Elektromos on les ellensúlyozza átmenet Zn + ionok az oldatban, így egy bizonyos száz-di- cink oldódási leáll.
Ilyen egyensúlyi állapot megfelel az egyenlő a két ható erők az ionok Zn +: kémiai, amelyek mellett a cink oldjuk, és az elektromos megelőzésére oldódás. Rust-megszűnik Vorenus cink jelenlétében egy poten-tial különbség? 1 közötti cink és nátrium.
Ha ugyanaz a megoldás az, hogy helyezze egy tányér egy másik anyagból, az ismertetett eljárás kerül sor ebben az esetben is. De kapott Nye potenciális különbség? 2. lehet más értéket - több vagy kevesebb? 1.
Ezen elv szerint van kialakítva, pl. d. a. az elektrokémiai cella és az akkumulátor (ábra. 2 a, b).
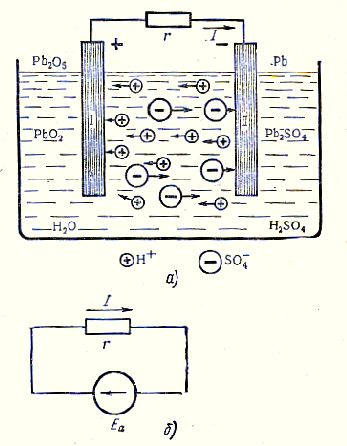
2. ábra: Az akkumulátor töltési mód ólom.
Amikor összekötő lemezeket I. és II egy zárt áramkört karmester jár e. d. a. kémiai elem
és elektromos áram jön létre.
Ebben az esetben pl. d. a. Ez hozza létre és tartja fenn működését elem kémiai erők (az oldalirányú erő), ezért beszélhetünk átalakításának kémiai energiát elektromos energiává alakítja.
Az elektromos áram a galván-cal elem kíséri visszafordíthatatlan elektrokémiai folyamatok, amelyek képes leírni ült meghatározott kémiai reakciókat.
Használata elektrokémiai cellák korlátozott - egy időben ők is adnak csak nezna-szignifikáns, villamos energia mennyisége-CIÓ, és a kifejezés munkájuk alacsony, és akkor végződik, amikor a hatóanyag az elektródok bizonyos mértékig fog izras-hodovano.
Szignifikánsan több-Application-set szükséges elemeket, elektro-kémiai folyamatokat, amelyek on-invertálható. Reverzibilitásának elektrokémiai folyamatok, iCal nezzunk dit ismételt töltés és időben egymás után elemeket. Amikor a töltés felhalmozódnak bizonyos mennyiségű kémiai energia miatt az elektromos energia és elvezetésére ez az energia lehet használni az elektromos áramkör formájában villamos energiát.